[Microbicidal activity of polihexanide]
Torsten Koburger 1Gerald Müller 2
Werner Eisenbeiß 3
Ojan Assadian 4
Axel Kramer 2
1 Hygiene Nord GmbH, Greifswald, Deutschland
2 Institut für Hygiene und Umweltmedizin der Ernst-Moritz-Arndt-Universität, Greifswald, Deutschland
3 Klinik für Plastische Chirurgie, Universitätsklinikum Schleswig-Holstein, Lübeck, Deutschland
4 Klinisches Institut für Hygiene und Medizinische Mikrobiologie, Medizinische Universität, Wien, Österreich
Abstract
When tested in the quantitative suspension test according to the prEN 12054, polihexanide meets the requirements defined by this standard for an antiseptic. At a product concentration of 0.02%, the test organisms are reduced by ≥5 lg, or ≥3 lg under dirty conditions, respectively, within a contact time of 5 min. This agrees well with the accepted recommendation of 0.02% polihexanide for the application on chronic wounds. In the presence of sesamoid bone/cartilage a polihexanide concentration of 0.005% is sufficient effective. As this concentration does not appear to have any adverse effects it might be promising to analyze its suitability for the antiseptic irrigation of joints in the animal model.
The combination of 0.1% polihexanide with undecylenamidopropyl betaine (Prontosan®) possesses the antiseptic properties specified above, too. However, with regard to the higher concentration of polihexanide, at least a repeated application of this formulation cannot be recommended for cleansing and irrigating wounds or burns.
Keywords
polihexanide, Lavasept®, Serasept®, microbicidal efficacy
Einleitung
Polihexanid (chemische Bezeichnungen N-Amidino-2-(2,6-dichlorphenyl)acetamid, Polyhexamethylenbiguanidhydrochlorid oder Poly(imino[imido-carbonyl]imino[imido-carbonyl] iminohexa-methylen)hydrochlorid)) (Abbildung 1 [Abb. 1]) enthält im Unterschied zu Chlorhexidin (Abbildung 2 [Abb. 2]) keine endständigen Chlorbenzensubstituenten.
Abbildung 1: Strukturformel von Polihexanid
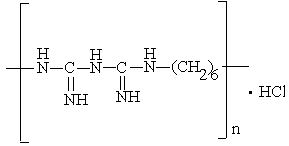
Abbildung 2: Strukturformel von Chlorhexidin
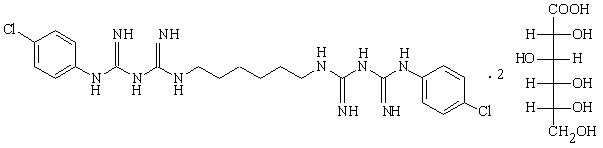
Es ist davon auszugehen, dass die im Vergleich zu Polihexanid mit Abstand ungünstigere Toxikologie (hohe Zytotoxizität, anaphylaktische und allergische Reaktionen, Neurotoxizität, Mutagenität) von Chlorhexidin auf diesem Strukturunterschied beruht.
Trotzdem ergibt sich aus bisherigen Untersuchungen, dass Polihexanid ohne und mit Belastung wirksamer als Chlorhexidin, bei hoher Blutbelastung auch wirksamer als lodophore ist, allerdings mit deutlich langsamerem Wirkungseintritt als bei lodophoren (erregerabhängig 5-20 min im quantitativen Suspensionstest [1]). Die Wirkung richtet sich auch gegen intrazellulär sich vermehrende Erreger wie Chlamydien und Neisserien [2]. Dieser Unterschied ist im Wirkungsmechanismus von Polihexanid begründet. Die mikrobiozide Wirkung beruht in erster Linie auf der selektiven Permeabilitätsbeeinflussung der bakteriellen Zellmembran auf Grund der starken Wirkung gegenüber sauren Phospholipiden bakterieller Zellmembranen bei nur geringer Beeinflussung neutraler Phospholipide humaner Zellmembranen [3], [4], [5]. Das führt zur Hemmung metabolischer Prozesse, die letztlich eine Koagulation des Zellinhalts nach sich ziehen [6], [7]. Hinzu kommt die Blockierung des mikrobiellen Attachments, nachgewiesen durch Hemmung dentaler Plaques [8] und durch remanente Wirkung bei Anwendung zur präoperativen Augenantiseptik [9].
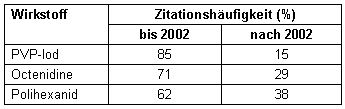
Im Ergebnis einer Medline-Analyse zur Zitationshäufigkeit von PVP-Iod und Octenidin im Vergleich zu Polihexanid ergab sich für den Zeitraum der letzten vier Jahre eine deutliche Zunahme zugunsten des letztgenannten Wirkstoffs (Tabelle 1 [Tab. 1]), was dessen zunehmende Bedeutung für die Praxis der Antiseptik widerspiegelt.
Tabelle 1: Zitationshäufigkeit von Polihexanid im Vergleich zu PVP-Iod und Octenidin
Daher sollten weitere Daten zur mikrobioziden Wirksamkeit von Polihexanid vor allem bei geringeren Konzentrationen generiert werden, um daraus möglicherweise Schlussfolgerungen für die Praxis der Antiseptik ableiten zu können.
Methoden
Die Testung wurde im quantitativen Suspensionstest gemäß EN 12054 [10] durchgeführt. Das Testprinzip besteht darin, dass 1 ml einer Suspension des Testorganismus (für Bakterien 108-109 Koloniebildende Einheiten (KbE)/ml, für C. albicans 107-108 KbE/ml) mit 9 ml der Prüflösung gemischt werden. Am Ende der Einwirkungszeit werden 1 ml aus dem Prüfsubstanz-Testorganismus-Gemisch in 9 ml Enthemmerlösung (3% Tween 80, 3% Saponin, 0,1% Histidin und 0,1% Cystein) überführt. Nach 5 min Neutralisation werden daraus und aus den dekadischen Verdünnungen dieses Prüfneutralisationsgemisches jeweils 1 ml als Doppelbestimmung auf CSL-Agar ausgespatelt und für 48 h bei 36°C kultiviert. Die Wirksamkeit wird in Form des Reduktionsfaktors (RF) ausgedrückt. Er wird berechnet aus der Differenz des lg der Anzahl KbE des Vor- und Nachwerts.
Die Verdünnungen der Prüfsubstanzen wurden jeweils mit sterilem destilliertem Wasser hergestellt.
Ergebnisse und Diskussion
Der Wirkstoff Polihexanid erfüllt gemäß [11] die Anforderungen an ein Antiseptikum ohne und mit organischer Belastung mit einem RF>5 (Tabelle 2 [Tab. 2]).
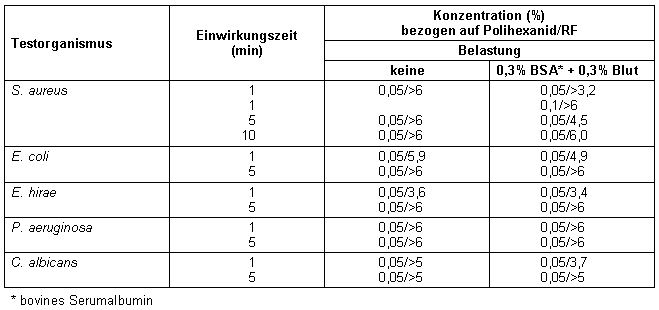
Tabelle 2: Mikrobiozide Wirksamkeit von Lavasept bzw. Serasept im quantitativen Suspensionstest
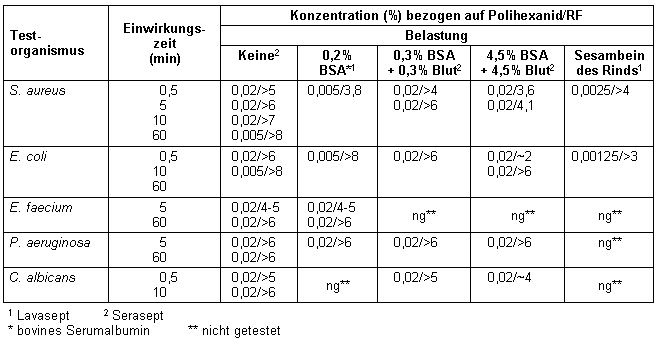
Aus den Ergebnissen geht hervor, dass Polihexanid bei 5 min Einwirkungszeit auch in der Verdünnung von 0,02%, wie sie zur Anwendung auf chronischen Wunden empfohlen wird, die Wirkungsanforderungen mit hohem Sicherheitsabstand an ein Antiseptikum erfüllt. In Gegenwart von Knorpel ist für die geprüften Testorganismen sogar eine Verdünnung von 0,005% ausreichend. Da diese Konzentration in vitro gerade noch knorpelverträglich ist [12], erscheint es aussichtsreich, ihre Effektivität und Verträglichkeit zur Gelenkspülung am Tiermodell zu untersuchen.
Die Kombination von 0,1% Polihexanid mit Undecylenamidopropylbetain (Prontosan®) erfüllt ebenfalls die Wirkungsanforderungen an ein Antiseptikum ohne und mit Belastung (Tabelle 3 [Tab. 3]).
Tabelle 3: Mikrobiozide Wirksamkeit der Kombination von 0,1% Polihexanid mit Undecylenamidopropylbetain (Prontosan
®
) im quantitativen Suspensionstest
Allerdings ist die Wirkstoffkonzentration 2,5 bis 5fach höher als im Lavasept® bzw. Serasept®, was mit einer höheren Zytotoxizität verbunden ist. Bei klinischer Anwendung wurde nach durchschnittlich 8tägiger Anwendung die Bildung gelber Membranen auf den Wunden auffällig, die als zytotoxische Reaktion aufzufassen sein dürfte.
Es zeigte sich im Einsatz von Prontosan bei Brandverletzungen, die länger als eine Woche mit einem Feuchtverband konservativ behandelt wurden, dass diese Membranen fest adhärent trocken auf den Wundoberflächen entstanden und eine weitere Reepithelialisierung nicht mehr stattfand. Das führte zur spätprimären operativen Behandlung mit tangentialer Exzision von trockenem Schorf inklusive oberster epithelialer Hautschichten und Spalthautdeckung von Arealen, die eigentlich spontan heilen sollten.
Der gleiche Prozess wurde auch unter längerer Prontosananwendung bei anderen Wundflächen beobachtet und führte dazu, dass Prontosan nicht mehr verwendet und wieder die konventionelle Lavasept-Konzentration bei Brandverletzungen eingesetzt wurde (Eisenbeiß pers Mitt.). Zumindest für Verbrennungswunden ist auf Grund dieser Beobachtungen der Einsatz von Prontosan nur zur einmaligen Wundreinigung zu empfehlen. Anschließend sollte die antiseptische Behandlung mit Lavasept® oder mit Serasept® fortgesetzt werden.
Literatur
[1] Werner HP, Kramer A. Mikrobiologische Anforderungen an lokale Antiinfektiva unter spezieller Berücksichtigung der antiinfektiven Wundbehandlung. In: Kramer A, Wendt M, Werner HP, Hrsg. Möglichkeiten und Perspektiven der klinischen Antiseptik. Wiesbaden: mhp; 1995. S. 26-30.[2] Jethon F, Kramer A. Verwendung von PHMB zur Behandlung von durch sich intrazellulär vermehrende Erreger verursachten Infektionen. EP 0788797 A1. 06.02. 1997.
[3] Ikeda T, Ledwith A, Bamford CH, Harm RA. Interaction of a polymeric biguanide biocide with phospholipid membranes. Biochim Biophys Acta. 1984;769:57-66.
[4] Ikeda T, Tazuki S, Watanabe M. Interaction of biologically active molecules with phospholipid membranes. 1. Fluorescence depolarization studies on the effect of polymeric biocide bearing biguanide groups in the main chain. Biochim Biophys Acta. 1983;735:380-6.
[5] Ikeda T, Tazuke S, Bamford C, Ledwith A. Spectroscopic studies on the interaction of polymeric in-chain biguanide biocide with phospholipids membranes as probed by 8-anilinonaphthalene-1-sulfonate. Bull Chem Soc Jpn. 1985;58:705-9.
[6] Davies A, Field BS. Action of biguanides, phenols and detergents on Escherichia coli and its spheroplasts. J Appl Bact. 1968;32:233-43.
[7] Mitchinson C, Pain RH, Vinson JR, Walker T. The relative effectiveness of guanidinium and some biguanide salts as denaturants. Biochim Biophys Acta. 1983;743:31-6.
[8] Rosin M, Welk A, Kocher T, Majic-Todt A, Kramer A, Pitten FA. The effect of a polyhexamethylene biguanide mouthrinse compared to an essential oil rinse and a chlorhexidine rinse on bacterial counts and 4-day plaque regrowth. J Clin Periodontol. 2002;98:392-9.
[9] Hansmann F, Kramer A, Ohgke H, Strobel H, Geerling G. Polyhexamethylbiguanid (PHMB) zur präoperativen Antisepsis bei Cataract Operation. Ophthalmologe. 2004;101:377-83.
[10] EN 12054. Chemical disinfectants and antiseptis - Quantitative suspension test for the evaluation of bactericidal activity of products for hygienic and surgical handrub and handwash used in human medicine - Test method and requirements (phase 2/step 1). Brüssel: European Committee for Standardization; 1997.
[11] Pitten FA, Werner HP, Kramer A. A standardized test to assess the impact of different organic challenges on the antimicrobial activity of antiseptics. J Hosp Infect. 2003;55(2):108-15.
[12] Müller G, Kramer A. Effect of selected wound antiseptics on adult articular cartilage (bovine sesamoid bone) in the presence of Escherichia coli and Staphylococcus aureus. J Orthop Res. 2005;23:127-33




