Biokompatibilitätsindex silberhaltiger Wundantiseptika
Gerald Müller 1Axel Kramer 1
Yousef Karkour 1
1 Ernst-Moritz-Arndt-Universität, Institut für Hygiene und Umweltmedizin, Greifswald, Deutschland
Zusammenfassung
Um die Wirksamkeit verschiedener Antiseptika miteinander vergleichen zu können, haben wir einen von uns als Biokompatibilitätsindex (BI) bezeichneten Quotienten eingeführt. Dieser Index berücksichtigt sowohl die Ergebnisse der In-vitro-Zytotoxizität, d.h. die Konzentration, bei der 50% der Zellen geschädigt werden (IC50), als auch die Mikrobiozidie, d.h. die Konzentration, bei der mindestens 5 log-Stufen Reduktion der Ausgangsdichte der eingesetzten Prüfmikroorganismen erzielt werden.
Für AgNO3 und Ag-SD ist kein BI-Wert zu berechnen, da die höchste geprüfte Wirkstoffkonzentration von 1% der Anwendungskonzentration entsprach und keine Reduktion der Ausgangserregerdichte auftrat. Der zu erwartende Wert müsste aber sehr viel kleiner als 0,002 sein. Sämtliche Ag-Präparate zeigten keine Reduktion der Ausgangsdichte von Staphylococcus aureus bei der Kontaktzeit von 30 min. Für kolloidales Silber in Form von mild silver protein (auf Ag bezogen) ergibt sich ein BI-Wert gegenüber Escherichia coli von 0,002, für Chlorhexidin 0,8, für PVP-Iod (auf Iod bezogen) 1,0, für Polihexanid 1,5 und für Octenidin 1,8, d.h. die Ag-haltigen Antiseptika besitzen innerhalb einer Kontaktzeit von 30 min keine antiseptische Wirkung. Sie sollten deshalb in der Praxis je nach Art der Wunde z.B. durch Polihexanid- , Octenidin- oder PVP-I- haltige Präparate ersetzt werden, die innerhalb von 30 min in geringerer Konzentration als der Anwendungskonzentration mikrobiozid wirksam sind.
Schlüsselwörter
In-vitro-Zytotoxizität, Biokompatibilitätsindex, Silbernitrat, Silbersulfadiazin, kolloidales Silber, Chlorhexidin, PVP-Iod, Polihexanid, Octenidin
Text
Zur Gruppe der Ag-haltigen Wundmittel zählt Silbernitrat (AgNO3), kolloidales Silber (besteht aus fein zerteiltem mit Eiweiß als Schutzkolloid versehenem, metallischem Silber), Silbersulfadiazin (Ag-SD) und Ag-haltige Wundauflagen.
Die mikrobiozide Wirksamkeit von Ag wird durch Ag+-Ionen erreicht. Gegenüber Bakterien wirkt Ag+, indem es die Zellwandaktivität beeinflusst, an bakteriellen subzellulären Bestandteilen bindet und diese zerstört, die Atmung inhibiert und essentielle Enzyme, die am Stoffwechsel von Na+, Mg2+ und Phosphat beteiligt sind, beeinträchtigt. Auch eine Inaktivierung bakterieller DNA und RNA wird beschrieben.
Die Nebenwirkungen bzw. Nachteile von Silber bestehen darin, dass Ag+ unerwünscht an Sulfhydryl-, Amino-, Imidazolyl-, Phosphat- und Carboxyl-Gruppen von Membran- und Enzymproteinen im Wundgewebe bindet und diese inaktiviert. Silber wird auch von den im Wundgebiet befindlichen Zellen aufgenommen. Ag kann somit in den systemischen Kreislauf gelangen und ggf. eine Argyrie hervorrufen.
Eigene Untersuchungen zeigten, dass kolloidales Silber in Form von mild silver protein (MSP) hinsichtlich der zytotoxischen Wirkung gegenüber Mäusefibroblasten (L929-Zellen, CCL 1) nach 30 min Kontaktzeit mit der Wirkung von PVP-Iod vergleichbar ist. Die zytotoxische Potenz von Chlorhexidin (CHex) ist mit der von AgNO3 und Ag-SD vergleichbar. Nach 30 min Kontaktzeit mit den Säugerzellen sind außerdem bei den Ag-haltigen Präparaten Silberablagerungen nachweisbar. Zum Vergleich wurden die IC50-Werte für CHex, Octenidin (Oct), Polihexanid (PHMB) und PVP-Iod (PVP-I) bestimmt sowie der Biokompatibilitätsindex berechnet (Tabelle 1 [Tab. 1]).
Tabelle 1: Mittlere IC
50
[µM] gegenüber L929-Zellen und Konzentration für einen Rf-Wert > 5 gegenüber
Escherichia coli
nach Kontakt über 30 min und der daraus berechnete Biokompatibilitätsindex für die verschiedenen Wirkstoffe von Wundantiseptika im Zellkulturmedium bei Anwesenheit von 10% fetalem bovinen Serum (FBS)
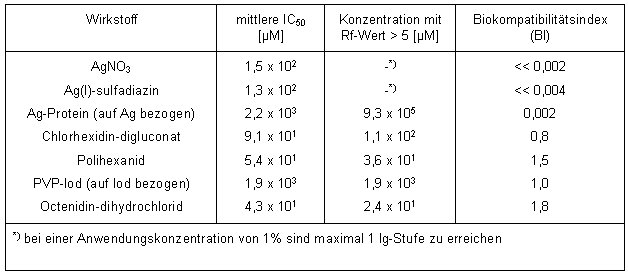
Um die Ergebnisse der Untersuchungen zur In-vitro-Zytotoxizität mit denen der Mikrobiozidie vergleichen zu können, wurden die gleichen Versuchsbedingungen gewählt, d.h. die Prüfsubstanzen befanden sich im Zellkulturmedium mit 10% FBS. Mittels quantitativem Suspensionstest oder Membranfiltration wurde die Konzentration bestimmt, bei der 5 log-Stufen Reduktion (Rf-Wert > 5) gegenüber den eingesetzten Prüfmikroorganismen erreicht wurden (Tabelle 1 [Tab. 1]).
Die Ag-haltigen Prüfpräparate AgNO3 und Ag-SD zeigten bei der Anwendungskonzentration von 1% keine geforderten 5-log-Stufen Reduktion. Im Gegenteil, sie waren gegenüber den Prüfmikroorganismen fast vollständig unwirksam. Nur 1% AgNO3 verminderte die Ausgangsdichte von Escherichia coli um maximal 1 log-Stufe. Sämtliche Ag-Präparate zeigten keine Reduktion der Ausgangsdichte von Staphylococcus aureus bei der Kontaktzeit von 30 min. Nur gegenüber Escherichia coli hatte die Prüfkonzentration von > 5% MSP einen Rf-Wert von 5 erreicht. Die gleichzeitig geprüften Wirkstoffe CHex, Oct, PHMB und PVP-I hatten bei Prüfkonzentrationen, die unterhalb ihrer Anwendungskonzentration lagen, Rf-Werte von 5 gegenüber beiden Prüfmikroorganismen (Tabelle 1 [Tab. 1]).
Um die Wirksamkeit verschiedener Antiseptika miteinander vergleichen zu können, haben wir einen von uns als Biokompatibilitätsindex (BI) bezeichneten Quotienten eingeführt. Dieser Index berücksichtigt sowohl die Ergebnisse der In-vitro-Zytotoxizität, d.h. die Konzentration, bei der 50% der Zellen geschädigt werden (IC50), als auch die Mikrobiozidie, d.h. die Konzentration, bei der mindestens 5 log-Stufen Reduktion der Ausgangsdichte bei den eingesetzten Prüfmikroorganismen erzielt werden.
Für AgNO3 und Ag-SD ist kein BI-Wert zu berechnen, da die höchste geprüfte Wirkstoffkonzentration von 1% der Anwendungskonzentration entsprach und keine Reduktion der Ausgangserregerdichte auftrat. Der zu erwartende Wert müsste aber sehr viel kleiner als 0,002 bzw. 0,004 sein. Für MSP (auf Ag bezogen) ergibt sich ein BI-Wert von 0,002, für CHex 0,8, für PVP-Iod (auf Iod bezogen) 1,0, für PHMB 1,5 und für Octenidin 1,8, d.h. die Ag-haltigen Antiseptika besitzen innerhalb einer Kontaktzeit von 30 min keine antiseptische Wirkung (Tabelle 1 [Tab. 1]). Möglicherweise entwickelt Ag+ seine mikrobiozide Wirksamkeit erst nach längerer Einwirkzeit auf die Mikroorganismen. Diese Vermutung wird durch In-vitro-Untersuchungen an der Wundauflage Actisorb Silver 220 bestätigt. Mit längerer Kontaktzeit der Wundauflage mit dem Prüfmikroorganismus Pseudomonas aeruginosa ist gleichzeitig eine stärkere Reduktion der KbE nachzuweisen. Nach 3 h Kontaktzeit war bereits eine Reduktion > 5 log-Stufen vorhanden [1].
Die Ag-haltigen Wundantiseptika sind wie folgt einzuschätzen:
- Sog. Ag-haltige Antiseptika, wie z.B. AgNO3 , Ag-SD und MSP, sind bei Anwesenheit von 10% FBS innerhalb von 30 min nicht antiseptisch wirksam, wohl aber noch zytotoxisch. Sie sollten in der Praxis je nach Art der Wunde z.B. durch PHMB-, Oct-haltige oder PVP-I- haltige Präparate ersetzt werden [2], die innerhalb von 30 min bereits in geringerer Konzentration als der Anwendungskonzentration mikrobiozid wirksam sind. Diese mikrobiozid wirksamen Konzentrationen werden von den Fibroblasten in vitro weitestgehend toleriert.
- Die mikrobiozide Wirkung von Ag+ besteht in einer Langzeitwirkung, wie sie auch von Ag-haltigen Wundauflagen ausgeht.
- Eine langsame und stetige Freisetzung von geringen Ag+-Mengen könnte zur Ausbildung von bakteriellen Resistenzen führen, wie es in der Publikation von Percival et al. [3] vorhergesagt wird.
Literatur
[1] Müller G, Winkler Y, Kramer A. Antibacterial activity and endotoxin-binding capacity of Actisorb Silver 220. J Hosp Infect. 2003;53(3):211-4.[2] Kramer A, et al. Konsensusempfehlung zur Auswahl von Wirkstoffen für die Wundantiseptik. Hyg Med. 2004;29:147-57.
[3] Percival SL, Bowler PG, Russell D. Bacterial resistance to silver in wound care. J Hosp Infect. 2005;60(1):1-7.
Erratum
Als Vorname des Autors Müller wurde irrtümlich "Georg" angegeben.




